هدف از جداسازی حذف ناخالصی ها ویا...

تبلور
هدف از تبلور ، جداسازی ناخالصی از اجسام جامد است. در این روش ، ابتدا جامد ناخالص را در یک حلال گرم حل میکنند، سپس محلول را صاف میکنند. ناخالصیها در فاز مایع باقی میمانند. اگر تبلور طی چند مرحله صورت گیرد، به آن تبلور جزء به جزء میگویند. در این روش انتخاب حلال از اهمیت بالایی برخوردار است. اگر از تکنیک ذوب برای جداسازی ناخالصی از جامد استفاده شود، به آن تصفیه ذوب گویند.این روش در جدا کردن ناخالصیهای ژرمانیم و اسید بتروییک کاربرد دارد. در این فرآیند ، ضریب تقسیم برابر با نسبت غلظت ناخالصی در فاز جامد به غلظت ناخالصی در فاز مایع است.
تقطیر
اگر هدف از تقطیر ، جداسازی یک مخلوط به اجزای بالا باشد، از تقطیر ساده برای جداسازی اجزاء استفاده میشود. اما اگر همه اجزاء فرار باشند، از تقطیر جزء به جزء برای جداسازی استفاده میشود. اگر یک مخلوط تولید آزئوتروپ کند، ( مثل آب و الکل) نمیتوان از روش تقطیر جزء به جزء ، اجزای آن را جدا کرد. برای جداسازی این مخلوط از روشهای تقطیر با بخار آب ، تقطیر در خلاء و تقطیر ناگهانی استفاده میکنند.در تقطیر با بخار آب هیچگاه درجه حرارت تقطیر از نقطه جوش آب بیشتر نمیشود. ترکیباتی نظیر تولوئن ، اتیلن ، گلیسیرین و اسیدهای چرب از این طریق جدا میشوند. برای جلوگیری از تجزیه مایعاتی که دارای نقطه جوش بالایی هستند از تقطیر در خلاء استفاده میشود. با کاهش فشار ، نقطه جوش مایع کاهش پیدا میکند.
در تهیه آب آشامیدنی از آب دریا و تهیه آب مقطر نیروگاهها از تقطیر ناگهانی استفاده میشود. در این روش مایع بطور مداوم وارد و بخار بطور مداوم خارج میشود.
رسوب دادن
نوعی روش جداسازی است که اساس آن اختلاف حلالیت اجسام میباشد. یعنی جزیی که حلالیت کمتری دارد زودتر جدا میشود. با افزایش نیروی جاذبه سرعت تهنشین شدن افزایش پیدا میکند. عمل سانتریفوژ در واقع بر همین اساس است.
استخراج
اساس این روش ، اختلاف حلالیت یک جزء در دو حلال غیر قابل حل در یکدیگر است. اگر دو حلال غیر قابل استخراج ، مایع باشند، به این روش استخراج مایع ـ مایع گویند و اگر یک جسم جامد به وسیله یک حلال استخراج شود، به آن استخراج جامد ـ مایع گویند (مثل استخراج اسانسها ، عصارهها و روغن از دانههای گیاهی). عموما دو فاز مورد استفاده ، یکی آب است و دیگری یک حلال آلی.مقداری از جسم در فاز آبی و مقداری نیز در فاز آلی میباشد. بازده استخراج با ضریب تقسیم نسبت مستقیم دارد. دوبار استخراج با حجم کمتر از حلال آلی همیشه موثر از یک بار استخراج با حجمی مساوی دو برابر حجم اول است. چون در حالت اول ، مقدار وزن ماده باقیمانده محلول در آب ، کمتر از حالت دوم خواهد بود.
کروماتوگرافی
اساس کروماتوگرافی ، جذب سطحی مواد و توزیع آنها در دو فاز میباشد. یکی از فازها ثابت و فاز دیگر متحرک است که نمونه مورد نظر در فاز متحرک جدا میشود. فاز ثابت یا جامد است و یا مایع و فاز متحرک یا مایع است و یا گاز . اگر فاز ثابت ، جامد و فاز متحرک ، مایع باشد، به آن کروماتوگرافی مایع ـ جامد ( LSC ) گویند. اگر فاز متحرک ، گاز و فاز ثابت ، جامد باشد، به آن کروماتوگرافی گاز - جامد ( GSC ) گویند. اگر فاز متحرک ، مایع و فاز ثابت نیز مایع باشد به آن کروماتوگرافی مایع ـ مایع ( LLC یا HPLC ) گویند و در نهایت اگر فاز متحرک ، گاز و فاز ثابت ، مایع باشد، به آن کروماتوگرافی گاز - مایع ( GLC یا VPC ) گویند.در LSC ، جدا شدن بر اساس جذب سطحی یا تعریض یونها و یا تشکیل کمپلکس میباشد. در GSC اساس ، جداسازی جذب سطحی است. در LLC و GLC ، مواد بر اساس توزیع بین دو فاز جدا میشوند. پس کروماتوگرافی روشی برای جداسازی مخلوط بدلیل اختلاف تحرک آنها میباشد.
کروماتوگرافی LSC در واقع نوعی کروماتوموگرافی جذبی است که مواد بر اساس اختلاف در قابلیت جذب خود روی سطح جامد از یکدیگر جدا میشوند. در GSC نیز اساس جداسازی جذب سطحی فاز گاز روی سطح جامد است. از این روش برای خالص سازی گازها استفاده میشود.

کروماتوگرافی تبادل یونی
کروماتوگرافی تبادل یونی ، روشی است که در آن ، یونها بین یک محلول و یک فاز جامد ( رزین ) مبادله میشوند. این تبادل ، برگشت پذیر است. فاز جامد در آب ، غیر محلول بوده و دارای بنیانهای اسیدی و بازی باشد. نوع معدنی این مواد جامد ، ممکن است شبیه زئولیتها باشند و نوع جدید آنها از مشتقات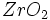 هستند و برای جداسازی فلزات قلیایی خاکی بکار میروند. رزینهای تبادل یونی ، منشا آلی دارند و از پلیمرهای با وزن مولکولی بالا ساخته میشوند.
هستند و برای جداسازی فلزات قلیایی خاکی بکار میروند. رزینهای تبادل یونی ، منشا آلی دارند و از پلیمرهای با وزن مولکولی بالا ساخته میشوند.تشکیل این رزینها بر اساس پلیمریزاسیون پلیاستیرن و وینیلبنزن استوار است. رزینها به دو نوع تعویض کننده آنیونی و کاتیونی تقسیم میشوند. هر کدام از این تعویض کنندهها به نوع بازی ضعیف و قوی و اسیدی ضعیف و قوی تقسیم میشوند.
تقطیر
تقطیر ، جداسازی مواد اجزای سازنده یک محلول با روش تبخیر و تراکم است.
اطلاعات اولیه
روش جداسازی مواد اجزای سازنده یک محلول گوناگونند. یکی از این روشها فرآیند تقطیر است که خود روشهای مختلفی دارد و از جمله کاربردهای مهم آن در پالایش نفت و جداسازی اجزای آن است.
انواع تقطیر
-
تقطیر ساده:اجزای سازنده محلولی از یک ماده حل شده غیر فعال را میتوان با تقطیر ساده از هم جدا کرد. برای این کار محلول را میجوشانیم تا حلال فرار ، تبخیر و از ماده حل شده جدا شود. با سرد کردن بخار ، (میعان) ، حلال مایع جمعآوری میشود و ماده حل شده به صورت باقی مانده تقطیر باقی میماند.
- تقطیر جزء به جزء:اجرای سازنده محلول شامل دو جز فرار را که از قانون رائولپیروی می کند، می توان با فرآیند تقطیر جزء به جزء از هم جدا کرد. طبق قانون رائول ، فشار بخار محلول برابر با مجموع اجزای بخار سازنده آن است و سهم هر جزء ، برابر با حاصلضرب کسر مولی آن جزء در فشار بخار آن در حالت خاص است.
مراحل تقطیر با استفاده از قانون رائول
در تقطیر محلولی از A و B ، غلضت A در بخاری که خارج شده و مایع میشود، بیش از غلظت آن در مایع باقیمانده است. با ادامه عمل تقطیر ، ترکیب درصد اجزا در بخار و مایع دائما تغییر میکند و این در هر لحظه عمومیت دارد. با جمع آوری مایعی که از سرد شدن بخار حاصل میشود و از تقطیر مجدد آن و با تکرار پی در پی این عمل ، سرانجام میتوان اجزای سازنده مخلوط اصلی را به صورتی واقعا خالص به دست آورد.انواع سیستمهای دارای انحراف از قانون رائول
-
سیستمهای که از قانون رائول انحراف مثبت دارند:در این
حالت در منحنی فشار کل ، ماکسیممی وجود دارد. این ماکسیم مربوط به محلولی ،
با ترکیب درصد معینی است که فشار بخار آن بالاتر از فشار بخار هر یک اجزای
خالص است. این نوع محلول که "محلول آزئوتروپ با نقطه جوش مینیمم" نام دارد، در دمایی به جوش میآید که پایینتر از نقطه جوش هر یک از اجزای آن در حالت خاص است.
- سیستمهای که از قانون رائول انحراف منفی دارند:اگر سیستمی انحراف منفی از قانون رائول نشان دهد، در منحنی فشار کل مینیممی وجود خواهد داشت. محلولی که غلظت متناظر با این مینیمم دارد، فشار بخاری خواهد داشت که در هر دمایی ، پایینتر از فشار بخار هر یک از اجزای آن در حالت خاص است. چنین محلولی در دمایی بالاتر از نقطه جوش هر یک از اجزای سازنده در حالت خاص ، میجوشد. این محلول ، "آزئوتروپ با نقطه جوش ماکسیم" نامیده میشود.
تعادل بخار با محلول آزئوتروپ
بخار در حالت تعادل با مایع آزئوتروپی چگونه به دست میآید؟بخار در حالت تعادل با مایع همگن که نقطه جوش ماکسیمم یا مینیمم دارد، دارای همان غلظتی است که مایع آن دارد. از این رو آزئوتروپها ، مانند مواد خالص ، بدون تغییر تقطیر میشوند. از محلول جز به جز یک محلول دو جزئی که آزئوتروپی تشکیل میدهند، سرانجام یک جزء خالص و آزئوتروپ حاصل میشود، ولی دو جزء آن ، بصورت خالص به دست نمیآید.
